7月3日,根據(jù)國(guó)家藥監(jiān)局官網(wǎng)公示��,杭州浩博醫(yī)藥開(kāi)發(fā)的反義寡核苷酸(ASO)藥物AHB-137擬納入突破性療法���,適應(yīng)癥為慢性乙型肝炎�。
7月3日��,根據(jù)國(guó)家藥監(jiān)局官網(wǎng)公示����,杭州浩博醫(yī)藥開(kāi)發(fā)的反義寡核苷酸(ASO)藥物AHB-137擬納入突破性療法,適應(yīng)癥為慢性乙型肝炎���。
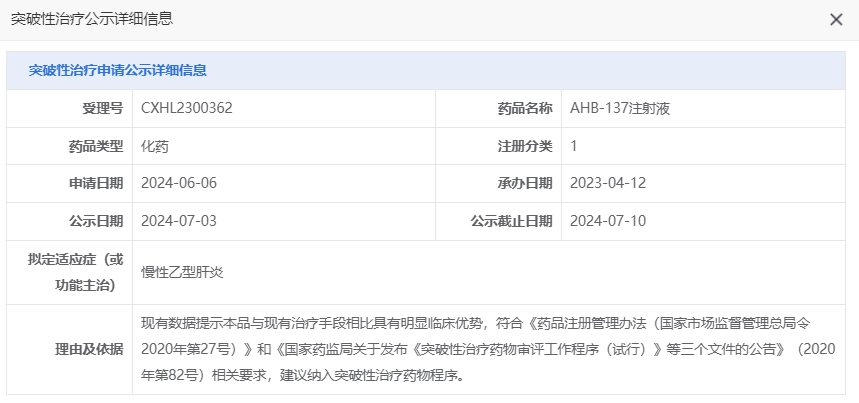
AHB-137是浩博醫(yī)藥基于自主研發(fā)平臺(tái)Med-Oligo™開(kāi)發(fā)����,具有潛力成為慢性乙型肝炎功能性治愈基石的非偶聯(lián)型的反義寡核苷酸(ASO)創(chuàng)新藥物����。在2024歐洲肝病學(xué)會(huì)年會(huì)(2024 EASL)上,公司披露了AHB-137兩項(xiàng)最新臨床研究進(jìn)展����,分別是針對(duì)中國(guó)大陸受試者的開(kāi)展的I/IIa期臨床(AB-10-8002)研究,以及國(guó)際多中心I期臨床(AB-10-8001)研究�。
LBP-019報(bào)告是來(lái)自AHB-137兩項(xiàng)正在進(jìn)行的I/IIa期臨床研究中健康受試者(HV)和CHB受試者的安全性和初步抗病毒活性數(shù)據(jù)。2項(xiàng)研究共有52例乙型肝炎e抗原(HBeAg)陰性����、接受穩(wěn)定核苷酸類(lèi)似物(NA)治療的CHB受試者被納入研究�, 44例受試者中14例來(lái)自AB-10-8001����,30例來(lái)自AB-10-8002。研究結(jié)果表明�,在基線HBsAg≤1,000IU/mL的CHB受試者中,150mg組中38%(3/8)的CHB受試者HBsAg下降≥1 log10IU/mL�,12%(1/8)的受試者HBsAg下降≥2 log10IU/mL;300 mg組中50%(10/20)的CHB受試者HBsAg下降≥1 log10IU/mL, 30%(6/20)的受試者HBsAg下降≥2 log10IU/mL���。
LBP-043報(bào)告披露了AB-10-8002臨床研究中的安全性和藥代動(dòng)力學(xué)(PK)數(shù)據(jù)���,研究結(jié)果表明:單劑量 AHB-137 吸收良好(Tmax為3.5-5.0h),消除緩慢(t1/2約85.2-106h)�。從75mg到450mg,血漿暴露量隨劑量增加而增加�。多次劑量組中未觀察到蓄積現(xiàn)象。
2. 肝臟時(shí)間:EASL2024:反義寡核苷酸 (ASO) AHB-137慢乙肝一期臨床數(shù)據(jù)顯示良好的HBsAg清除療效與安全性




![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2024 上海博華國(guó)際展覽有限公司版權(quán)所有(保留一切權(quán)利)
滬ICP備05034851號(hào)-57
2006-2024 上海博華國(guó)際展覽有限公司版權(quán)所有(保留一切權(quán)利)
滬ICP備05034851號(hào)-57